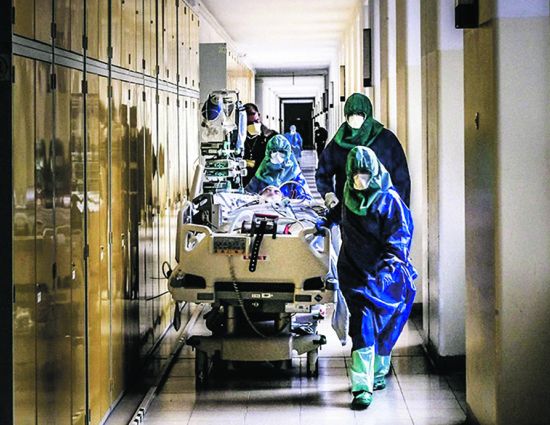
Regulador europeu anuncia sexta-feira se aprova a vacina da Pfizer para jovens dos 12 aos 15 anos
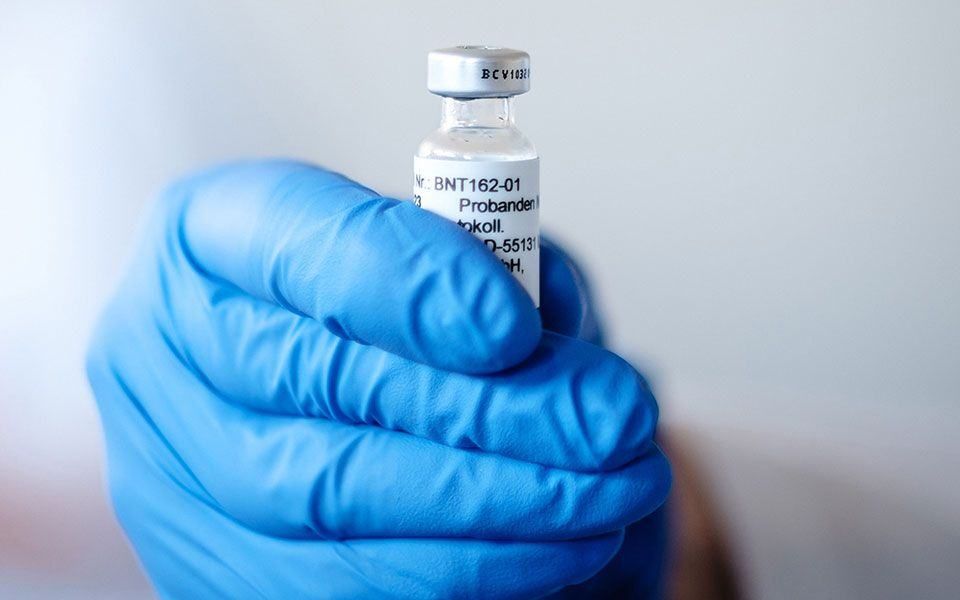
A Agência Europeia de Medicamentos (EMA) vai anunciar, esta sexta-feira, se aprova o pedido de autorização condicional de comercialização da Pfizer/BioNTech para crianças dos 12 aos 15 anos.
De acordo com a agência francesa “AFP”, caso seja aprovada, será a primeira vacina a receber luz verde para os jovens nos 27 países da União Europeia. Até agora, a vacina desta dupla farmacêutica está apenas autorizada para pessoas com mais de 16 anos.
“O resultado da reunião extraordinária do comité de medicina humana da EMA… para discutir a indicação pediátrica para a Comirnaty [nome comercial da vacina]” será divulgado numa conferência esta sexta-feira, cita a agência um email oficial.
Nos Estados Unidos e no Canadá, a vacina, intitulada de Comirnaty, já foi aprovada pelo regulador Food and Drug Administration (FDA) para esta faixa etária. A aprovação na União Europeia estava prevista inicialmente para junho, depois de a EMA ter anunciado no início deste mês que aguardava dados dos testes clínicos das farmacêuticas e de um estudo realizado no Canadá.
A autorização surgiu na sequência do resultado dos ensaios clínicos de fase 3 que contou com 2.260 participantes de 12 a 15 anos de idade, onde se registou uma eficácia de 100%.
“Os resultados deste ensaio, anunciados a 31 de março de 2021, mostraram uma eficácia vacinal de 100% nos participantes com ou sem infeção prévia por SARS-CoV-2 e respostas robustas de anticorpos. No ensaio, a vacina também foi geralmente bem tolerada. Os participantes continuarão a ser monitorizados para uma proteção e segurança a longo prazo por mais dois anos após a sua segunda dose”, refere o documento.
Esta terça-feira, a Moderna anunciou que também o seu fármaco registou uma eficácia de 100% entre os jovens desta faixa etária, estando agora a preparar um pedido de autorização à FDA e à EMA que deverá ficar formalizado já em junho.
RECOMENDADO
Tagus Park – Edifício Tecnologia 4.1
Avenida Professor Doutor Cavaco Silva, nº 71 a 74
2740-122 – Porto Salvo, Portugal
online@medianove.com